適切に実施されたランダム化比較試験(randomized controlled trial:RCT)の報告は,蓄積されて知識ベースを構成し,エビデンスを 明らかなものにすることによって,安全で有効なヘルスケアの基礎となる.しかし,その中でかなりの割合が投稿されておらず,この 知識ベースに寄与していない1,2).これらは出版バイアス(publication bias)と呼ばれ,患者の健康管理にとって重要な 意味を持ってくる.
第1に,治療効果がポジティブである試験ほど投稿される可能性が高い.このため,出版された試験のみにもとづき研究を統合する ことは,治療効果についての結論を誤る可能性があり,患者を無効であるばかりか有害ですらある治療に晒すことになる3).
第2に,試験の報告が少ないと,中等度ではあるが臨床的に重要な治療効果を検出するためのシステマティック・レビュー (systematic review)の検出力を減ずることになる.結果として,患者が効果的な種類のヘルスケアを受けられないことが起こりうる.
第3に,試験を報告しないことは,研究の参加者に対する研究者の倫理義務に反するものである.
第4に,試験が報告されないがために,患者はすでに答えが得られている疑問に答えるための新たな試験に参加を要請されるかも しれない4).
本稿では,まず出版バイアスの簡単な紹介,ついでそれを見出すためのファンネル・プロット法,さらに未公表の試験を捜して登録する amnestyの試みについて,紹介する.
1.出版バイアス
有意な結果を報告している臨床試験が出版されやすいことはすでに報告されている.DickersinとMinは,臨床試験の有意な結果とその 出版の有無についての関連を調べた4つの研究のメタアナリシスを行った1).結果が有意な試験は,有意でない試験に 対して約3倍出版されていた.彼らは他の要因は,出版とは明確な関連がないことに気付いた.割付法の隠蔽 (allocation concealment)やintension-to-treat解析(ITT解析)のような研究方法論の点については,出版の有無との関連はなかった. このメタアナリシス研究では,質の低い試験が出版されない試験であるということは明らかではなかった.その代わりにDickersinと Minは,試験が報告されない最も一般的な理由は,研究者が「結果が面白くない」,あるいは「十分な時間がなかった」と考えるからである ことを見出した.
2.ファンネル・プロット
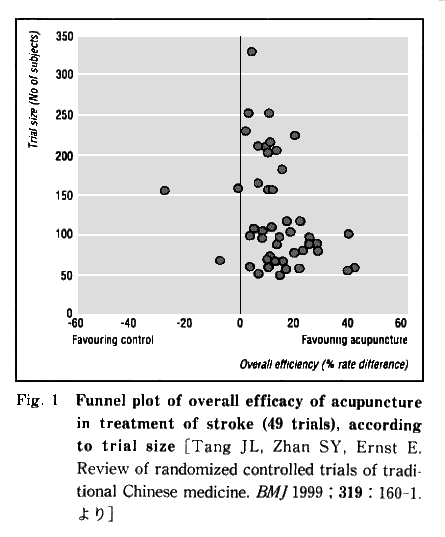 ファンネル・プロット(funnel plot)は,システマティック・レビューにおいて出版バイアスや他の選択バイアスの存在を評価するために
使われている.Fig. 1の例に示すように,ファンネル・プロットは通常,横軸に試験の治療効果,例えばオッズ比や有効率の差などを示し,
縦軸には治療効果の精度(precision),それは多くは標本の大きさの関数として表されるが,この2次元上に臨床試験の結果がプロットされる.
プロットの形は通常,逆さまの漏斗のようになるはずである.しかし,期待される治療効果が小さければ小さいほど,試験は投稿される
可能性が低くなる.その結果,出版バイアスが存在する場合,ファンネル・プロットの下方の片側は空白となる.本来そこには利益を示唆
しない少数例の試験の結果が存在しているべきものである3).
ファンネル・プロット(funnel plot)は,システマティック・レビューにおいて出版バイアスや他の選択バイアスの存在を評価するために
使われている.Fig. 1の例に示すように,ファンネル・プロットは通常,横軸に試験の治療効果,例えばオッズ比や有効率の差などを示し,
縦軸には治療効果の精度(precision),それは多くは標本の大きさの関数として表されるが,この2次元上に臨床試験の結果がプロットされる.
プロットの形は通常,逆さまの漏斗のようになるはずである.しかし,期待される治療効果が小さければ小さいほど,試験は投稿される
可能性が低くなる.その結果,出版バイアスが存在する場合,ファンネル・プロットの下方の片側は空白となる.本来そこには利益を示唆
しない少数例の試験の結果が存在しているべきものである3).Eggerらは,ファンネル・プロットの非対称性に関する回帰分析法を開発した5).その分析法の妥当性は,メタアナリシスの 結果と大規模臨床試験の結果とを比較して評価された.彼らは回帰分析法が有意である時,つまり出版バイアスや選択バイアスが存在 している可能性が高い時は,メタアナリシスの結果が大規模臨床試験の結果と一致しないことを示した.出版バイアスや他の選択バイアス のため,心筋梗塞の患者はマグネシウムで長らく不適切に治療され,また心不全の患者も硝酸塩で治療されてきたが,いずれの薬剤も 効果的でなく,副作用をもつ治療であるということをEggerらの結果は示唆している.また, Annals of Internal Medicine, BMJ, JAMA, The Lancet の4つの主要な医学雑誌のメタアナリシスの38%,そしてコクランライブラリの メタアナリシスの13%で有意なファンネル・プロットの非対称性を見いだした.
3.Medical Editors Trial Amnesty(META)とは
3-1 METAの発足と方法
 1997年の秋に,幾つかの国際的な医学雑誌の編集者らが,出版されない臨床試験の救済(amnesty)を求めるために会議をチェコの
プラハで開催した.そのアイディアは単純なものである.このamnestyに参加している医学雑誌は,読者である研究者に対し,報告されて
いない試験を登録フォームに記載し,返送することを強く勧める論説を発表した.登録フォームの例をFig. 2<PDF form>に示す.
1997年の秋に,幾つかの国際的な医学雑誌の編集者らが,出版されない臨床試験の救済(amnesty)を求めるために会議をチェコの
プラハで開催した.そのアイディアは単純なものである.このamnestyに参加している医学雑誌は,読者である研究者に対し,報告されて
いない試験を登録フォームに記載し,返送することを強く勧める論説を発表した.登録フォームの例をFig. 2<PDF form>に示す.このプロジェクトは医学雑誌の編集者(medical editor)による臨床試験(trial)の救済(amnesty)であるところから Medical Editors Trial Amnesty(医学雑誌編集者による臨床試験の救済:META)と呼ばれる.
試験の登録は可能な限り単純にし,最小限の情報(連絡先,試験参加者数,被験者のタイプ(病気の種類),介入の種類)とされた. こうして,たとえ実際のデータを送ることが不可能であるとしても,登録に関する情報を送ることは誰でも可能となった.重複登録の程度も 予測された.登録フォームは,論説を掲載している雑誌の編集事務局に,郵送,ファクスあるいは電子メール(meta@ucl.ac.uk)で送られる. その雑誌の編集部は返送された用紙をチェックし,それらをamnestyのオーガナイザーへ送る.
これらの試験情報をインターネットウェブ上に詳細に掲載したり,コクランライブラリに収載したりして,公的に利用可能となるように するのである.システマティック・レビューを行う人,あるいは新しい研究をデザインする人が,もし特定の試験データが必要ならば, レビューアーは試験リストから直接この情報を探し出し,それを登録した人に連絡をすることが可能となった.
3-2 METAのインパクト
現時点(1999年12月)で,amnestyに関する論説は50以上の医学雑誌で発表されている.コクランライブラリには35,000人以上の 被験者を含むおよそ180のランダム化比較試験が登録されている.
また,このamnestyは未公表試験の問題全般に注意を引くこととなった.例えば,このamnestyに応えて英国医療研究評議会 (Medical Research Council:MRC)は,結果を公的に利用可能にする範囲を評価するために,MRCがスポンサーした全ての試験を 調査追跡することとなった.いくつかの国では,製薬産業がスポンサーした臨床試験の出版率は公的スポンサーのもとに比して低いことが 指摘されている.
このamnestyは,非企業分野また企業分野の研究者にも,共によい機会を提供することになる6).英国では,英国製薬 工業協会(Association of British Pharmaceutical Industry:ABPI)がこのamnestyの活動に応えるよう要請されている7,8). 保健省とABPIの間の任意協定である薬価調整システムにおいて,製薬産業の研究開発に対する政府助成金が効果的に使われるべき ことを考慮すれば,このamnestyを用いることは特に適切なものとなる.
おわりに
METAは,出版バイアスの問題への完全な解答というわけではない.これはすでに実施された臨床試験を「後ろ向き」に救済するもの である.1948年に報告された世界で最初のRCT以降,過去半世紀蓄積されてきた偏った報告による,患者への有害な影響を防ぐことは, 大きな課題であろう.これに対応するのがamnestyである.
研究資金提供者,倫理委員会,研究者,雑誌編集者のamnestyに対する支持は,報告されない試験の課題に対処するために,重要な 要因である.
一方,臨床試験の開始時にそれを「前向き」に登録公開することは,将来の出版バイアスを避けるためには,大きい可能性を持つ. コクラン共同計画10)の,出版されているもの,未出版のものを問わずすべてのランダム化比較試験を集積する努力は, こうした過去の試験,将来の試験の登録に関して,すでにある程度の影響を持ちつつあるといえる.
ひるがえって,日本の現状を考えてみよう.これまで日本では出版バイアスに関する議論はあまりされてこなかった.唯一,「臨床評価」誌が 1972年の創刊から,いわゆるネガティブトライアルも掲載する編集方針を持っており,「発刊の辞」に「本誌は薬効判定に止まらず,商品価値が ないとされている無効論文や副作用報告,および臨床のほかの分野の地味な研究を中心に組み,…(中略)…とくにスポンサーが 消極的なために報告されるべくして,埋もれている貴重なデータを可能な限り掲載し,一部の専門家による情報独占の弊害を主体的に減少 させる場として行きたい」とある.このことは,世界的にも歴史的にもより注目されていいものである.現在のようなシステマティック・レビューや メタアナリシスの方法が開発され,そこで出版バイアスの弊害が論議される時代に,この編集方針は再びその意義をもつものである.
出版バイアスは,世界的レベルで考えられるべきものである.2,500以上の医学雑誌が日本で出版されているが,MedlineあるいはEMBASE のどちらかに収載されているのはわずか約300誌にすぎない.日本には約1万のRCTが存在するが,コクランライブラリには約2,000 が収載されているにすぎない.この状況を打開すべく日本のRCTをコクランライブラリに収載するプロジェクトが進行中である11). そのうちには,「臨床評価」誌に載ったネガティブトライアルも含まれる.しかし日本においてネガティブな結果が発表されるのは,おそらく まれなことであろう.
日本のRCTを世界的に活用するための活動と同時に,日本においてこれまで実施されたもののうち未公表臨床試験を,組織的に捜す 必要がある.また臨床試験の前向きの登録・公開を含めて,日本の行政,医療従事者,企業,雑誌編集者のこの方面への貢献が世界的にも 求められているのである12,13).
日本の雑誌編集者でこのMETAに参加したところはまだないようである.日本でこれまでに臨床試験に関わり,この領域に関心ある方は, しばらくはFig. 2<PDF form>に示した英文のフォームを用い,BMJ などに送付してもらいたい.近いうちに日本の医学雑誌編集者でMETAに 参加するところがあらわれることが望まれる.
謝 辞
METAに参加した医学編集者に謝意を表する.
1) Dickersin K, Min YI. NIH clinical trials and publication bias. On-line J Curr Clin Trials [serial online]1993;Apr 28:Doc No 50.
2) Easterbrook PJ, Berlin JA, Gopalan R, Matthews DR. Publication bias in clinical research. Lancet 1991;337:867-72.
3) Egger M, Davey Smith G. Misleading meta-analysis. BMJ 1995;310:752-4.
4) Savulescu J, Chalmers I, Blunt J. Are research ethics committees behaving unethically? Some suggestions for improving performance and accountability. BMJ 1996;313:1390-3.
5) Egger M, Davey Smith G, Schneider M, Minder C. Bias in meta-analysis detected by a simple, graphical test. BMJ 1997;315:629-34.
6) Wise P, Drury M. Pharmaceutical trials in general practice: the first 100 protocols. A audit by the clinical research ethics committee of the Royal College of General Practitioners. BMJ 1996;313:1245-8.
7) Roberts I. Pharmaceutical industry is invited to respond to amnesty for unreported trials. BMJ 1997;315:683.
8) Maynard A, Bloor K. Regulating the pharmaceutical industry. BMJ 1997;315:200-1.
9) Chalmers I. Underreporting research is scientific misconduct. JAMA 1990;263:1405-8.
10) 津谷喜一郎,中山健夫,柳 元和,金子善博.コクラン共同計画:その展開と今後の展望.薬剤疫学 1999;4(2):185-98.
11) 津谷喜一郎,廣瀬美智代,栗原千絵子,平田智子,他.日本のRCT論文をThe Cochrane Library/CENTRALに収載するには. 医学図書館2000;47(1):68-76.
12) 津谷喜一郎.うまい話には気をつけよ−sound criticismの形成を−.In:シンポジウム「高度先進医療とEBM」(1999.2.26). 高度先進医療 平成11年度号 2000:265-77.
13) 津谷喜一郎.公表要件廃止問題と承認申請資料に関する日米欧三極の状況〜公表要件廃止問題.ICHとCTD〜.In:薬害オンブス パースンタイアップグループ設立二周年記念シンポジウム(1999.11.3)報告書.「薬の情報公開〜日米の比較を通じて〜」.薬害オンブス パースンタイアップグループ,2000:7-15.レジュメは,(http://www.yakugai.gr.jp/news/tsutani.html).